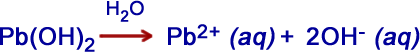V - Acidez e basicidade dos compostos químicos
Abaixo a representação de uma dissociação iônica (separação de íons) de uma base:
M(OH)x -> Mx+ + XOH-
Onde:
- M -> Metal (cátion)
- OH -> Hidroxila (ânion)
- x -> número de hidroxilas que invertido de baixo para cima à esquerda, corresponderá à carga do metal (positiva).
Hidróxido de amônio (NH4OH): uma base diferente
O hidróxido de amônio (NH4OH) é a única base que não apresenta metal em sua fórmula sendo proveniente do borbulhamento da amônia (NH3) em água:

O hidróxido de amônio (NH4OH) é a única base volátil (possui baixo ponto de ebulição).
Exemplo da dissociação iônica do hidróxido de sódio:
O hidróxido de sódio é uma substância sólida que na presença de água, libera os íons Na+ (cátion) e OH– (ânion) que se dissolvem devido à atração pelos pólos negativos e positivos da molécula de H2O.
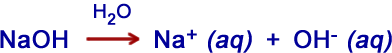
OBS: aq (aquoso), na presença de água.
Através dos exemplos abaixo podemos entender melhor como ocorre à dissociação iônica de uma base na presença de água, ou seja, em meio aquoso (aq):
Hidróxido de cálcio
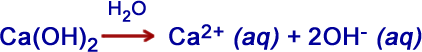
Hidróxido de alumínio

Hidróxido de chumbo IV ou plúmbico
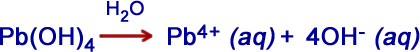
Hidróxido de chumbo II ou plumboso