IV - Como ocorrem as reações químicas?
4.1.1 Ruptura homolítica ou homólise
Na cisão homolítica, a ligação covalente quebra em partes iguais, ficando cada átomo ligante com um elétron desemparelhado (livre), obtendo como resultado dois radicais.
As espécies resultantes são eletricamente neutras e chamadas de RADICAIS OU RADICAIS LIVRES.
Para que ocorra a homólise de uma ligação covalente é necessário fornecer energia (calor, luz etc.) para o sistema, ou então é necessária a presença de outro radical livre no meio.

LEMBRE-SE: O RADICAL LIVRE É ELETRICAMENTE NEUTRO.
1º Exemplo - Molécula de metano (CH4)
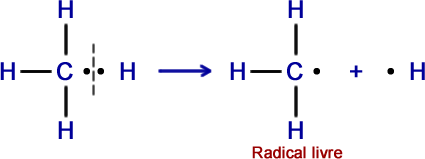
- Os radicais formados são altamente reativos;
- A grande reatividade dos radicais deve-se a tendência dos elétrons livres de se tornarem emparelhados através da formação de íons ou de ligações covalentes;
- No exemplo, o radical metil é tão reativo que não pode ser armazenado;
- O elétron isolado é indicado por um ponto no átomo de C de .CH3.
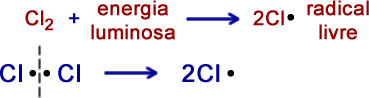
2º Exemplo - Molécula de cloro (Cl2)